カリウムはあらゆる細胞・生命にとって不可欠なミネラルです。例えば動物において、カリウムイオン(K+)は、神経や心臓の拍動を支え、その濃度異常が、てんかんや不整脈を引き起こします。これらのはたらきは、K+がイオンチャネル(注1)を“通って”細胞内外を移動するためであることが広く知られていましたが、イオンチャネルの働きを切り替える“スイッチ”として機能する仕組みは知られていませんでした。今回、生理学研究所の下村拓史助教(研究当時)(現:広島大学大学院医系科学研究科)、久保義弘教授、名古屋市立大学大学院薬学研究科の鈴木力憲講師、東京都医学総合研究所の齋藤実プロジェクトリーダーらのグループは、動物においてはじめて、細胞外のK+を“スイッチ”として直接感知するチャネル分子を発見しました。本研究結果は、Nature Communications誌(2026年4月22日18時)に掲載されました。
カリウムは細胞からなるすべての生命に必須のミネラルです。ヒトを含む動物では、体液中(細胞外)のカリウムイオン(K+)濃度の異常はてんかんや不整脈につながるため、その濃度は厳密に制御されています。K+の濃度は、細胞膜に存在するイオンチャネルなどの膜タンパク質(注2)を介した、K+の細胞内外への移動(透過)を通じて調整されています(図1左)。
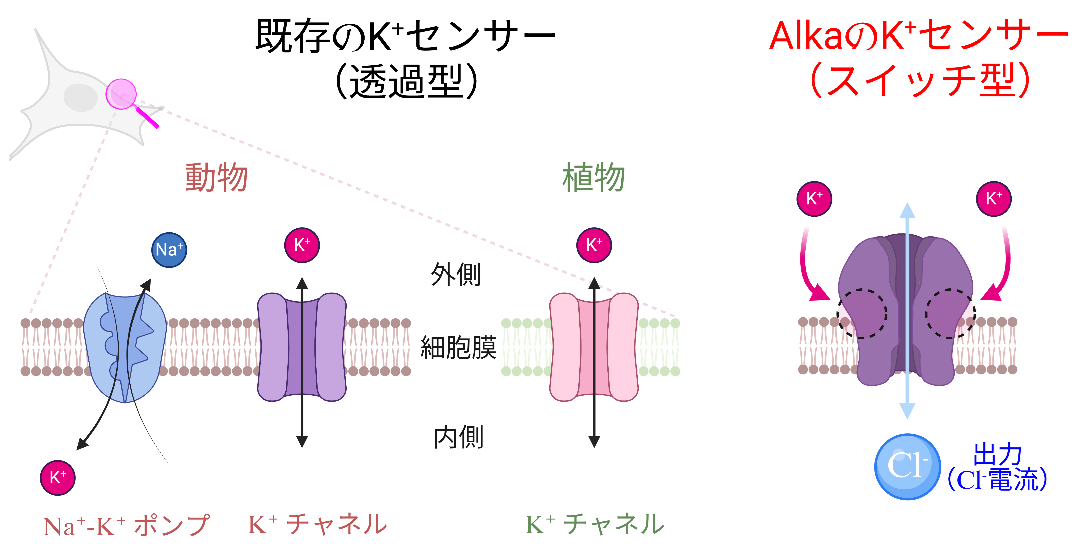
図1 Alkaは細胞外のK+を“スイッチ”として結合する
(左)これまで、K+の恒常性に関わる膜タンパク質は、K+自体を細胞膜を超えて透過させる機能を持つことが知られていました。(右)今回、塩化物イオン(Cl-)チャネルであるAlkaは、細胞外のK+を結合する領域を持ち、その結合に応じて、K+とは異なる出力であるCl-の細胞膜透過を制御することが明らかになりました。
イオンチャネルが開閉し、イオンを通すかどうかを決める“スイッチ”には様々なものがありますが、重要な“スイッチ”の一つが、特定の分子(リガンド)がチャネルに結合することです。この結合が“スイッチ”となりチャネル開閉の変化を引き起こし、電流の変化などを生み出します。
これまで、K+は、単にイオンチャネルを透過する対象であるだけで、チャネルにとって“スイッチ”としての役割は無いと考えられており、実際、動物や植物において、K+がスイッチとして働く明確なものは、イオンチャネルのみならず膜タンパク質一般で今まで見つかっていませんでした。
本研究において、ショウジョウバエの脳に存在するAlkaと呼ばれるイオンチャネルが、細胞外K+をスイッチとして認識する受容体であることを発見しました(図1右)。
研究グループは、まずAlkaを発現させた細胞の電気活動を記録し、同時に細胞外のK+濃度を変化させたところ、K+濃度によってチャネル電流が変化することを明らかにしました(図2)。この結果は、細胞外K+がリガンドとしてAlkaに結合し、Alkaの開閉を変化させ、電流の変化を引き起こしたことを示唆しています。
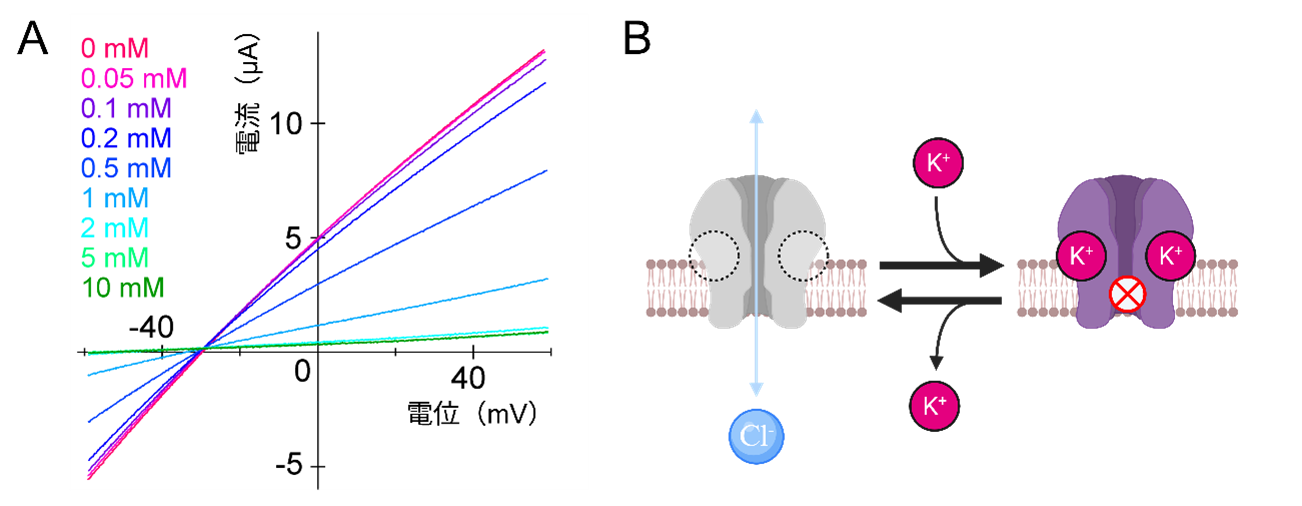
図2 細胞外K+によるAlkaチャネル電流の変化
細胞外K+濃度を上昇させると、Alkaを流れる電流量は減少しました(A)。これは、K+が結合すると、Cl-電流が流れなくなるような状態にAlkaチャネルの状態が変化することを示しています(B)。
そこで次に、Alkaのどの部分に、細胞外K+が結合するのかを検討するため、近年急速に発展した生成AI技術を用いたタンパク質立体構造予測プログラム(注3)と電気生理学的解析を組み合わせて調べました。その結果、AlkaのK+結合領域は、K+が水溶液中で安定的に存在している状態と極めて似た環境を原子レベルで作りだすことで、K+を結合できるようにしていることがわかりました(図3)。これは、2003年のノーベル化学賞受賞理由ともなったK+チャネルのK+選択性・透過性のメカニズムとよく類似しています。このように、細胞外K+を結合し、異なる出力(チャネル電流)を生じることが明確に確認された膜タンパク質は、動物も含め真核生物では初めての例です。
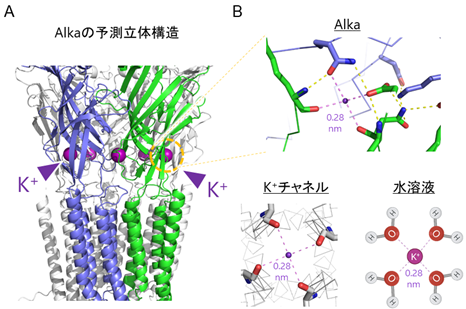
図3 AlkaがK+を認識する原子レベルでのメカニズム
(A) Alkaの予測立体構造モデル。Alkaに相当する部分はリボンで、結合したK+は紫色の球であらわしています。(B) Alka予測構造におけるK+結合領域と、他の環境でのK+との比較。赤い棒は酸素原子。K+は水溶液中では水分子に包まれ、エネルギー的に安定な距離・配置で酸素原子と結合します(右下)。AlkaとK+チャネルは、この水溶液中の環境を再現するような立体構造を持つことで、K+を結合できるようにしていることが明らかになりました。
では、ヒトの体の中でもK+が同様の働きをする可能性はあるのでしょうか?この疑問に答えるため、さらに研究グループは、ヒトの脳に存在し、Alkaとよく似たイオンチャネルであるグリシン受容体が、細胞外K+により制御されるかどうかを調べました。一般的なタイプのグリシン受容体はK+濃度の変化に影響されることはありませんでしたが、興味深いことに、RNA編集(注4)により性質が変化したタイプでは、K+の濃度によってチャネル電流が変化することがわかりました(図4)。このことは、K+が“スイッチ”として働くしくみが、ハエから進化的に遠く離れたヒトでもある程度残存していることを示します。
下村講師は「本研究によって、細胞外K+濃度を感知する分子メカニズムとして、“透過”タイプだけではなく、“スイッチ”タイプが存在することが明らかになりました。これをきっかけに、新たな細胞外K+恒常性メカニズムが発見され、てんかんなど病気との関連や、これらK+依存性チャネルを標的とした治療薬の開発などにつながるかもしれません。」と話しています。
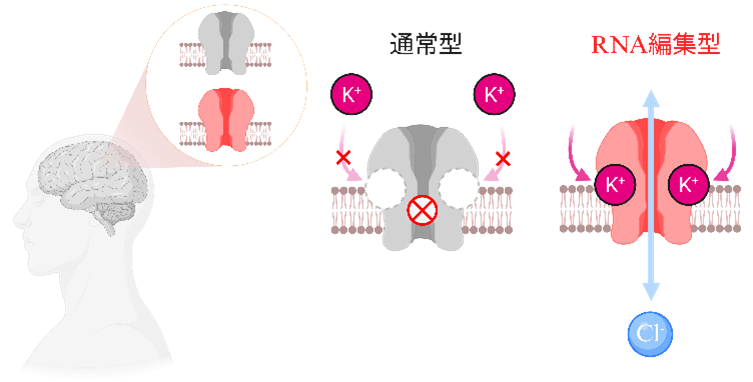
図4 RNA編集型のヒトグリシン受容体はK+による制御を受ける
(左)ヒトの脳内に存在するグリシン受容体は、通常のタイプと、RNA編集を受けたタイプが存在します。(右)通常タイプはK+によって影響を受けない一方で、RNA編集を受けたタイプは、細胞外K+濃度に応じてCl-電流が変化することが明らかになりました。
※図は一部Biorender.comを利用して作成しました。
注1)イオンチャネル:細胞膜に存在するタンパク質の一種で、特定のイオンを選択的に通すことができる。これにより、神経や筋肉のはたらきの基盤となる、細胞内外の電気的なバランスが作られる。
注2)膜タンパク質:細胞の内外を区切る膜に埋め込まれて存在するタンパク質。細胞の内外をつなぐ“通路”や“センサー”として働き、物質の出入りや情報のやり取りを担う。
注3)タンパク質立体構造予測プログラム:タンパク質の機能を理解するために重要な立体構造を計算機により予測する手法。近年、機械学習や生成AIの発展により予測精度が大きく向上し、実験結果と遜色のない高精度な予測が可能となった。これが評価され、2024年のノーベル化学賞の受賞理由の一つとなった。
注4)RNA編集:遺伝子DNAをもとに作られたRNAの情報を書き換える細胞の仕組み。これにより、同じ遺伝子から異なる性質をもつタンパク質が作られることがある。
本研究は文部科学省科学研究費補助金、住友財団、豊秋奨学会、上原記念生命科学財団の補助を受けて行われました。
1.動物において、細胞外K+で開閉するイオンチャネル分子を初めて発見し、そのK+結合メカニズムを解明
2.ヒトのイオンチャネルでも、同様のメカニズムが残存していることを発見
3.細胞外K+が細胞機能を調節する新しいシグナルとして働く可能性を示唆
体液中のK+濃度は極めて厳密な濃度(3-5 mM以内)に制御される必要がありますが、てんかんでは、K+濃度が異常なレベルに高くなることがあります。本研究で見いだされたK+をスイッチとして認識するタイプのグリシン受容体は、側頭葉てんかん患者の脳では多く存在していることから、こうしたグリシン受容体タイプの変化は、病的なK+濃度の変化に対処するメカニズムなのかもしれません(図4)。本研究をもとに、こうした細胞外K+に応答する新しいメカニズムや病気との関連が明らかになり、これらを標的とした治療薬の開発につながることも期待されます。
<論文タイトル・著者情報>
Extracellular K+ modulates the pore conformations of Cys-loop receptor anion channels.
Takushi Shimomura, Yoshihiro Kubo, Minoru Saitoe & Yoshinori Suzuki*.
*:責任著者
Nature Communications. (日本時間2026年4月22日18時掲載)
DOI: 10.1038/s41467-026-71629-z




