高齢HER2陽性早期乳がんでHER2DXが長期予後を予測―RESPECT試験トランスレーショナル解析(Trans-RESPECT)―
研究成果の概要
高齢(70~80歳)のHER2陽性早期乳がん(注1)は、化学療法による副作用リスクが相対的に高く、抗HER2療法(トラスツズマブ)に化学療法を上乗せするべき患者を見極めることが重要です。
本研究(Trans-RESPECT)は、日本で実施された第III相ランダム化比較試験RESPECT(トラスツズマブ単独 vs トラスツズマブ+化学療法)に参加した患者検体を用いて、HER2陽性早期乳がん向け多遺伝子アッセイ「HER2DX」(注2)の臨床的有用性を検討しました。
その結果、HER2DXリスク分類(低リスク/高リスク)が長期転帰と関連し、低リスク群で10年転帰が良好であること、さらに多変量解析でも全生存期間(OS)(注3)と独立して関連することが示されました。
探索的解析では、HER2DXのpCR4スコア高値群で化学療法上乗せが有益となる可能性も示唆されました。
本研究(Trans-RESPECT)は、日本で実施された第III相ランダム化比較試験RESPECT(トラスツズマブ単独 vs トラスツズマブ+化学療法)に参加した患者検体を用いて、HER2陽性早期乳がん向け多遺伝子アッセイ「HER2DX」(注2)の臨床的有用性を検討しました。
その結果、HER2DXリスク分類(低リスク/高リスク)が長期転帰と関連し、低リスク群で10年転帰が良好であること、さらに多変量解析でも全生存期間(OS)(注3)と独立して関連することが示されました。
探索的解析では、HER2DXのpCR4スコア高値群で化学療法上乗せが有益となる可能性も示唆されました。
研究のポイント
•RESPECT試験参加の中の154例でHER2DXを評価(低リスク74.0%、高リスク26.0%に層別化)。
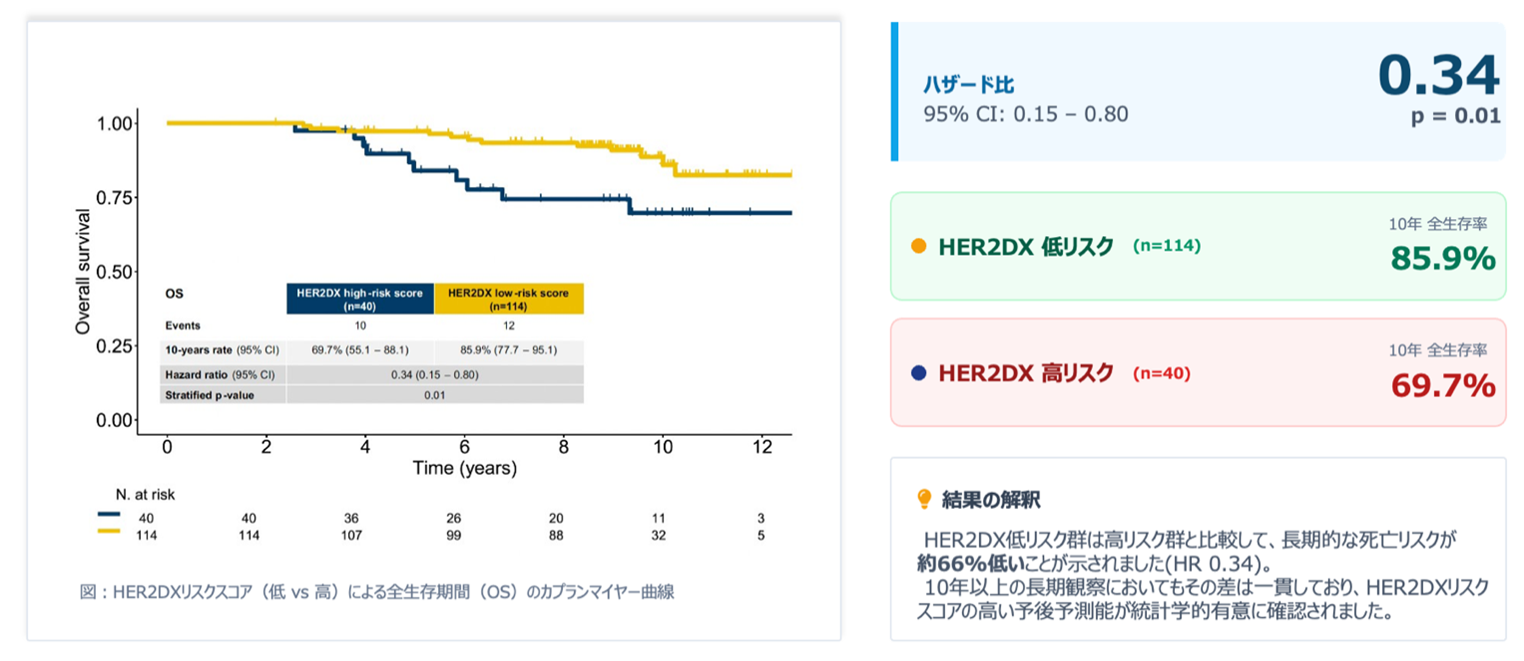
•低リスク群は高リスク群に比べ、10年転帰が良好で、全生存期間(OS)で有意差を確認。
•多変量解析でもHER2DXリスク群はOSと独立して関連し、高齢患者における治療強度最適化の判断材料となる可能性。
•探索的に、pCRスコア高値群で化学療法上乗せの有益性が示唆。
•低リスク群は高リスク群に比べ、10年転帰が良好で、全生存期間(OS)で有意差を確認。
•多変量解析でもHER2DXリスク群はOSと独立して関連し、高齢患者における治療強度最適化の判断材料となる可能性。
•探索的に、pCRスコア高値群で化学療法上乗せの有益性が示唆。
背景
HER2陽性早期乳がんでは、トラスツズマブと化学療法の併用が標準治療として確立しています。一方、高齢者では毒性や併存疾患の影響により、治療の個別化が特に重要です。RESPECT試験は高齢(70~80歳)を対象に、トラスツズマブ単独と化学療法併用を比較した試験ですが、臨床現場で「誰に化学療法を上乗せすべきか」をよりに判断するための指標が求められていました。
研究の成果
本解析では、HER2DXリスクスコアにより長期転帰が層別化され、低リスク群で良好な10年転帰が示されました。特にOSにおいて、HER2DX低リスク群が有意に良好でした。さらに年齢、腫瘍径、リンパ節転移、ホルモン受容体、治療群などを調整した多変量解析でも、HER2DXリスク群はOSと独立して関連を認めました。
また探索的解析として、HER2DX pCRスコア高値群で化学療法上乗せが有益となる可能性が示唆されました。
また探索的解析として、HER2DX pCRスコア高値群で化学療法上乗せが有益となる可能性が示唆されました。

研究の意義と今後の展開や社会的意義など
本研究は、エビデンスが限られやすい高齢HER2陽性早期乳がんにおいて、HER2DXが長期予後の層別化に有用であることを示しました。
これにより、化学療法を省略しても良好な転帰が期待できる患者と、化学療法上乗せが有益となり得る患者の同定に資する可能性があります。今後は、治療効果の予測(pCRスコアなど)について、より大規模な検証や前向き研究での確認が望まれます。
これにより、化学療法を省略しても良好な転帰が期待できる患者と、化学療法上乗せが有益となり得る患者の同定に資する可能性があります。今後は、治療効果の予測(pCRスコアなど)について、より大規模な検証や前向き研究での確認が望まれます。
用語解説
(注1)HER2陽性乳がん: HER2タンパクが過剰発現している乳がん。全乳がんの約15-20%を占める
(注2)HER2DX: HER2陽性早期乳がんに特化した多遺伝子アッセイ。27遺伝子の発現を解析し、リスクスコアとpCRスコアを算出
(注3)全生存期間(OS):死亡までの期間。
(注4)pCR(病理学的完全奏効): 術前化学療法後に腫瘍が完全に消失した状態
(注2)HER2DX: HER2陽性早期乳がんに特化した多遺伝子アッセイ。27遺伝子の発現を解析し、リスクスコアとpCRスコアを算出
(注3)全生存期間(OS):死亡までの期間。
(注4)pCR(病理学的完全奏効): 術前化学療法後に腫瘍が完全に消失した状態
研究助成
本研究は、がん臨床研究事業(CSPOR)、中外製薬株式会社、およびReveal Genomics社の支援を受けて実施されました。
論文情報
【論文タイトル】
HER2DX in older patients with HER2-positive early breast cancer: extended follow-up from the RESPECT trial of trastuzumab ± chemotherapy
【著者】
Kazuki Nozawa1,2, Masataka Sawaki3, Yukari Uemura4, Michiko Tsuneizumi5, Toshimi Takano6, Naomi Gondo7, Fumikata Hara8, Michiko Harao9, Tatsuya Toyama2, Naruto Taira10, Ana Vivancos11, Charles M. Perou12, Esther Sanfeliu11, Fara Brasó-Maristany11, Joel S. Parker11, Wesley Buckingham11, Laia Paré11, Guillermo Villacampa13, Mercedes Marín-Aguilera11, Patricia Villagrasa11, Aleix Prat11,14-17,*, Hiroji Iwata1,*
所属
1.名古屋市立大学大学院医学研究科 臨床研究戦略部 先端医療・臨床研究開発学分野
2.名古屋市立大学大学院医学研究科 乳腺外科学分野
3.国立病院機構 名古屋医療センター ブレストセンター・乳腺外科
4.国立国際医療研究センター 臨床研究センター データサイエンス部 生物統計研究室
5.静岡県立総合病院 乳腺外科
6.公益財団法人がん研究会有明病院 乳腺内科
7.相良病院 乳腺・甲状腺外科
8.愛知県がんセンター 乳腺科
9.自治医科大学 乳腺腫瘍内科
10.川崎医科大学 乳腺・甲状腺外科学
11.Reveal Genomics, Barcelona, Spain.
12.Department of Genetics, Lineberger Comprehensive Cancer Center, University of North Carolina, Chapel Hill, NC, USA.
13.Statistics Unit, Vall d'Hebron Institute of Oncology, Barcelona
14.Translational Genomics and Targeted Therapies in Solid Tumors, August Pi i Sunyer Biomedical Research Institute (IDIBAPS), Barcelona, Spain.
15.Department of Medical Oncology, Clínic Barcelona Comprehensive Cancer Center, Barcelona, Spain.
16.Breast Cancer Unit, IOB-QuirónSalud, Barcelona, Spain.
17.Department of Medicine, University of Barcelona, Spain.
(*Corresponding author)
【掲載学術誌】
学術誌名:Nature Communications
DOI番号:10.1038/s41467-025-65599-x
HER2DX in older patients with HER2-positive early breast cancer: extended follow-up from the RESPECT trial of trastuzumab ± chemotherapy
【著者】
Kazuki Nozawa1,2, Masataka Sawaki3, Yukari Uemura4, Michiko Tsuneizumi5, Toshimi Takano6, Naomi Gondo7, Fumikata Hara8, Michiko Harao9, Tatsuya Toyama2, Naruto Taira10, Ana Vivancos11, Charles M. Perou12, Esther Sanfeliu11, Fara Brasó-Maristany11, Joel S. Parker11, Wesley Buckingham11, Laia Paré11, Guillermo Villacampa13, Mercedes Marín-Aguilera11, Patricia Villagrasa11, Aleix Prat11,14-17,*, Hiroji Iwata1,*
所属
1.名古屋市立大学大学院医学研究科 臨床研究戦略部 先端医療・臨床研究開発学分野
2.名古屋市立大学大学院医学研究科 乳腺外科学分野
3.国立病院機構 名古屋医療センター ブレストセンター・乳腺外科
4.国立国際医療研究センター 臨床研究センター データサイエンス部 生物統計研究室
5.静岡県立総合病院 乳腺外科
6.公益財団法人がん研究会有明病院 乳腺内科
7.相良病院 乳腺・甲状腺外科
8.愛知県がんセンター 乳腺科
9.自治医科大学 乳腺腫瘍内科
10.川崎医科大学 乳腺・甲状腺外科学
11.Reveal Genomics, Barcelona, Spain.
12.Department of Genetics, Lineberger Comprehensive Cancer Center, University of North Carolina, Chapel Hill, NC, USA.
13.Statistics Unit, Vall d'Hebron Institute of Oncology, Barcelona
14.Translational Genomics and Targeted Therapies in Solid Tumors, August Pi i Sunyer Biomedical Research Institute (IDIBAPS), Barcelona, Spain.
15.Department of Medical Oncology, Clínic Barcelona Comprehensive Cancer Center, Barcelona, Spain.
16.Breast Cancer Unit, IOB-QuirónSalud, Barcelona, Spain.
17.Department of Medicine, University of Barcelona, Spain.
(*Corresponding author)
【掲載学術誌】
学術誌名:Nature Communications
DOI番号:10.1038/s41467-025-65599-x
